Carbocation vs Carbanion
Nøgleforskellen mellem carbocation og carboanion er deres ladninger; de er begge organiske molekylære arter med modsatte ladninger. Carbocation er positivt ladet ion og carboanion er negativt ladet ion. Deres stabilitet afhænger af flere faktorer, og nogle af dem er meget vigtige i syntesen af andre kemiske forbindelser.
Hvad er Carbocation
En carbocation er en kemisk art, som bærer en positiv ladning på et kulstofatom. Dens navn giver den klare idé, at det er en kation (en positiv ion), og ordet carbo refererer til et kulstofatom. Carbocation omfatter flere kategorier; primær carbocation, sekundær carbocation og tertiær carbocation. De er klassificeret efter antallet af alkylgrupper knyttet til det positivt ladede carbonatom. Deres stabilitet og reaktivitet varierer afhængigt af disse substituenter.

Carbocation Stabilitetstendens
Hvad er Carbanion
En carboanion er en organisk molekylær art med en negativ elektrisk ladning placeret på et kulstofatom. Med andre ord er det en anion, hvor et carbonatom har et udelt elektronpar med tre substituenter. Dets samlede antal valenselektroner er lig med otte. De dannes ved at fjerne positivt ladede grupper eller atomer fra et neutr alt molekyle. De er meget vigtige som kemiske mellemprodukter til at syntetisere andre stoffer såsom plast og polyethylen (eller polyethylen). Den mindste carbanoin er 'methide ion' (CH3–); dannet af metan (CH4) ved tab af en proton (H–).

Hvad er forskellen mellem Carbocation og Carbanion?
Karakteristika ved Carbocation og Carbanion
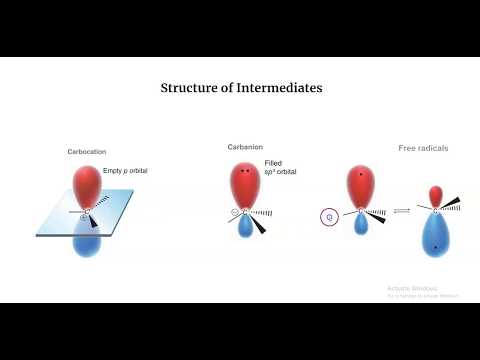
Carbocation: Carbocation er sp2 hybridiseret, og den ledige p-orbital ligger vinkelret på planet af tre substituerede grupper. Derfor har den en trigonal plan molekylær struktur. Carbocation kræver et elektronpar for at fuldføre oktetten. De kan reagere med nukleofiler, kan deprotoneres fra en pi-binding og kan have omarrangementer i den samme art.
Carbanion: En alkylcarboanion har tre bindingspar og et ensomt par; så dens hybridisering er sp3, og geometrien er pyramideformet. Geometrien af allyl- eller benzylcarboanion er plan, og hybridiseringen er sp2 Oktetten er komplet i den yderste kredsløb af et carboanionisk carbonatom, og den opfører sig som en nukleofil til at reagere med elektrofiler.
Stabilitet:
Carbocation: Carbocation-stabilitet afhænger af forskellige faktorer. Det er mere stabilt, når flere -R-grupper er knyttet til det positive carbonatom. Derfor er tertiær carbocation forholdsvis stabil end primære.

Resonansstrukturer øger også stabiliteten.
Carbanion: Carboanions stabilitet afhænger af flere faktorer; Elektronegativitet af carbanionisk carbon, resonanseffekt, induktiv effekt forårsaget af vedhæftet substituent og stabilisering af >C=O, –NO2 og CN grupper til stede på carbanionisk carbon
Definitioner:
Indukteffekt: Det kan være eksperimentelt observerbar effekt af transmission af ladning gennem en kæde af atomer i et molekyle, hvilket resulterer i en permanent dipol i en binding.
Eksempler på Carbocation og Carbanion
Carbocation:
Primær Carbocation:

I en primær (1°) carbocation er det positivt ladede carbonatom kun bundet til én alkylgruppe og to hydrogenatomer.
Sekundær Carbocation:

I en sekundær (2°) carbocation er det positivt ladede carbonatom bundet til to andre alkylgrupper (som kan være ens eller forskellige) og et hydrogenatom.
Tertiær kulsyre:

I en tertiær (3°) carbocation er det positive carbonatom bundet til tre alkylgrupper (som kan være en hvilken som helst kombination af ens eller forskellige), men ingen hydrogenatomer.
Carbanion:
Carboanion er også klassificeret i tre kategorier på samme måde som i carbocation; primær carboanion, sekundær carboanion og tertiær carboanion. Det gøres også baseret på antallet af –R-grupper knyttet til det anioniske carbonatom.