Nøgleforskel – Isoelektrisk vs Isoionisk punkt
De to termer isoelektrisk punkt og isoionisk punkt beskriver det samme biokemiske koncept om aminosyrer; det isoelektriske punkt eller det isoioniske punkt er den pH, hvor de positive ladninger af en aminosyre er lig med de negative ladninger af den samme aminosyre. Der er således ingen forskel mellem udtrykkene isoelektrisk punkt og isoionisk punkt.
Hvad er isoelektrisk punkt eller isoionisk punkt?
Isoelektrisk punkt eller isoionisk punkt for en aminosyre er den pH-værdi, ved hvilken de positive ladninger af en aminosyre er lig med de negative ladninger af den samme aminosyre. Det er angivet med pI. Da der ikke er nogen netto elektrisk ladning i aminosyren, kan den ikke migrere i et elektrisk felt. Derfor er isoelektrisk punkt det punkt, hvor aminosyren er neutral.
Ved isoelektrisk punkt dannes en zwitterion. En zwitterion er et dipolært molekyle, der har mere end to funktionelle grupper med positive og negative ladninger (positivt ladede funktionelle grupper og negativt ladede funktionelle grupper). De positive ladninger på funktionelle grupper bør være lig med de negative ladninger, der er til stede på funktionelle grupper af aminosyren. Dette gør den elektriske nettoladning af zwitterionen nul.

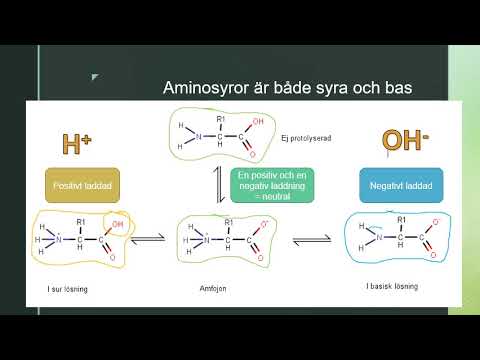
Figur 01: De sure, basiske og neutrale former for en aminosyre
På det isoioniske punkt er zwitterionen den dominerende form af aminosyren. pI-værdien kan opnås ved at bruge pKa-værdierne for netto positiv ladning og netto negativ ladning af aminosyrerne i sure og basiske medier.
Hvis der ikke er ladede funktionelle grupper i sidekæden af aminosyren,
pI=½(pKa1 + pKa2) hvor pKa1 og pKa 2 er pKa-værdierne for aminosyren i sure og basiske medier.
- Hvis der er sure sidekæder, er pI lavere end forventet.
- Hvis der er grundlæggende sidekæder, er pI højere end forventet.
Hvad er forskellen mellem isoelektrisk og isoionisk punkt?
Isoelektrisk punkt, også kendt som det isoioniske punkt, af en aminosyre er den pH-værdi, ved hvilken de positive ladninger af en aminosyre er lig med de negative ladninger af den samme aminosyre, angivet med pI
Oversigt – Isoelektrisk vs Isoionisk punkt
Der er ingen forskel mellem udtrykkene isoelektrisk punkt og isoionisk punkt. Begge udtryk bruges til at navngive den pH-værdi, ved hvilken der ikke er nogen netto elektrisk ladning i en aminosyre.